Содержание
- Как бороться с коррозией металла
- Ремонт своими руками: как покрасить, чтобы после первой же зимы не полезла ржавчина?
- Тема: «Коррозия металлов и меры борьбы с ней». Занятие 1.
- Виды коррозии металла и борьба с ней
- 1 Разновидности ржавления
- 2 Что наиболее часто ржавеет и как от этого предохраняться
- 3 Что делать, если ржавчина уже есть
- 4 Почему надо бороться со ржавчиной
- Заказ звонка
- Как избавиться от коррозии на металлических конструкциях
Как бороться с коррозией металла
Как бороться с коррозией металла
КОРРОЗИЯ МЕТАЛЛОВ И СПЛАВОВ
1. Коррозия (от латинского « corrodere » разъедать) – самопроизвольный окислительно-восстановительный процесс разрушения металлов и сплавов вследствие взаимодействия с окружающей средой.
2. Виды коррозии: химическая и электрохимическая
I . Химическая – коррозия, обусловленная взаимодействием металлов с веществами, содержащимися в окружающей среде, при этом происходит окислительно-восстановительное разрушение металла без возникновения электрического тока в системе.
К химической коррозии относятся:
— газовая коррозия — коррозионное разрушение под воздействием газов при высоких температурах;
— коррозия в жидкостях-неэлектролитах.
— химическая коррозия, обусловленная взаимодействием металлов с газами.
Основной окислитель – кислород воздуха.
Процессы химической коррозии железа:
2 Fe + O 2 = 2 FeO
3 Fe + 3 O 2 = FeO · Fe 2 O 3 (смешанный оксид железа ( II , III ) )
4 Fe + 3 O 2 + 6 H 2 O = 4 Fe ( OH )3 (на воздухе в присутствии влаги)
Fe ( OH )3 t ° C → H 2 O + FeOOH (ржавчина)
2 Fe + 3 Cl 2 = 2 FeCl 3
Химическая коррозия в жидкостях-неэлектролитах
Жидкости-неэлектролиты — это жидкие среды, которые не являются проводниками электричества. К ним относятся: органические (бензол, фенол, хлороформ, спирты, керосин, нефть, бензин); неорганического происхождения (жидкий бром, расплавленная сера и т.д.). Чистые неэлектролиты не реагируют с металлами, но с добавлением даже незначительного количества примесей процесс взаимодействия резко ускоряется. Например, если нефть будет содержать серу или серосодержащие соединения (сероводород, меркаптаны) процесс химической коррозии ускоряется. Если вдобавок увеличится температура, в жидкости окажется растворенный кислород — химическая коррозия усилится.
Присутствие в жидкостях-неэлектролитах влаги обеспечивает интенсивное протекание коррозии уже по электрохимическому механизму.
Химическая коррозия в жидкостях-неэлектролитах подразделяется на несколько стадий:
— подход окислителя к поверхности металла;
— хемосорбция реагента на поверхности;
— реакция окислителя с металлом (образование оксидной пленки);
— десорбция оксидов с металлом (может отсутствовать);
— диффузия оксидов в неэлектролит (может отсутствовать).
Для защиты конструкций от химической коррозии в жидкостях-неэлектролитах на ее поверхность наносят покрытия, устойчивые в данной среде.
II . Электрохимическая – окислительно-восстановительное разрушение сплавов и металлов, содержащих примеси, с возникновением электрического тока в системе.
АНОД (более активный металл) – разрушается
КАТОД (менее активный металл или примесь неметалла, способного + ē) – восстанавливается среда
Ме 0 – n ē → Me n + (процесс окисления)
кислая среда: 2 H + + 2ē → H 2 (процесс восстановления)
влажный воздух: O 2 + 2 H 2 O + 4ē → 4 OH — (процесс восстановления)
Электрохимическая коррозия железной детали с примесями меди во влажном воздухе.
А: Fe 0 — 2ē → Fe 2+ (Окисление)
К: O 2 + 2 H 2 O + 4ē → 4 OH — (процесс восстановления)
Итог: 2 Fe + O 2 + 2 H 2 O = 2 Fe ( OH )2 (белая ржавчина)
4 Fe ( OH )2 + 2 H 2 O + O 2 = 4 Fe ( OH )3 (бурая ржавчина)
1). Металлические покрытия – анодное (покрытие более активным металлом Zn , Cr ) – оцинкованное железо; катодное (покрытие менее активным металлом Ni , Sn , Ag , Au ) – белая жесть (лужёное железо) – не защищает от разрушения в случае нарушения покрытия.
2). Неметаллические покрытия – органические (лаки, краски, пластмассы, резина — гумирование, битум);
3). Протекторная защита – присоединение пластины из более активного металла ( Al , Zn , Mg ) – защита морских судов.
4). Электрохимическая (катодная) защита – соединение защищаемого изделия с катодом внешнего источника тока, вследствие чего изделие становится катодом. Ток идёт в противоположном направлении.
5). Добавление ингибиторов ( в зависимости от природы металла – NaNO 2, Na 3 PO 4, хромат и бихромат калия, ВМС органические соединения), адсорбируются на поверхности металла и переводят его в пассивное состояние.
Задания и вопросы по теме: «Коррозия металлов и сплавов»
№1. При электрохимической коррозии на поверхности анода протекает процесс
А) Восстановления ионов водорода; Б) Окисления металла;
В) Восстановление молекул кислорода; Г) Окисления молекул водорода.
№2. Почему считают, что рядом со стальной коронкой (Fе) не рекомендуется ставить золотую (Аu)?
№3. Вот история, произошедшая с норвежским грузовым судном «Анатина». Трюмы теплохода, направлявшегося к берегам Японии, были заполнены медным концентратом. Корпус судна сделан был из стали. Внезапно судно дало течь. Объясните, что произошло.
№4. Какой из компонентов загрязненного городского воздуха является наиболее коррозионно-активным по отношению к металлам, особенно при повышенной влажности:
а) N2; б) СО; в) SO2.
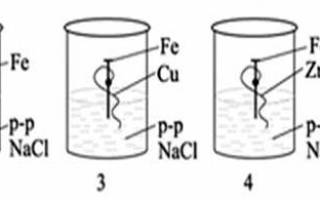
№5. Рассмотрите рисунок, ответьте на вопросы:
Обратите внимание! В восстановлении кислорода участвуют ионы Н + . Если концентрация Н + понижается (при повышении рН), восстановление О2 затрудняется. Замечено, что железо, находящееся в контакте с раствором, рН которого выше 9–10, не корродирует.
С усилением коррозии в присутствии солей часто сталкиваются автомобилисты в тех местностях, где в зимнее время для борьбы с гололедицей дороги обильно посыпают солью. Влияние солей объясняется тем, что образуемые ионы создают электролит, необходимый для возникновения замкнутой электрической цепи.
- Определить тип коррозии в каждом стакане.
- В каких стаканах железный гвоздь прокорродировал сильнее, в каких меньше, а в каких коррозии не подвергся? Почему?
- Объясните, что усиливает коррозию, а что ее замедляет?
№6. Рассмотрите процесс коррозии при соединении медной трубы с гальванизированной (оцинкованной) стальной трубой, если обе трубы находятся в земле.
№7. Почему цинк не используют при изготовлении консервных банок для покрытия им железа? Почему оцинкованное железо идёт на изготовления вёдер, баков?
№8. Как будет протекать процесс коррозии в том случае, если железную водосточную трубу прибить к дому алюминиевыми гвоздями?
№9. При изготовлении луженого железа (белой жести) — железо покрывают оловом, какое это покрытие — А) Анодное; Б) Катодное? Запишите электродные процессы
№10. Знаменитая Кутубская колонна в Индии близ Дели вот уже полторы тысячи лет стоит и не разрушается, несмотря на жаркий и влажный климат. Сделана она из железа, в котором почти нет примесей. Объясните, почему в данном случае статуя не подвергается коррозии
Ремонт своими руками: как покрасить, чтобы после первой же зимы не полезла ржавчина?
Этот вопрос на разных формах зачастую звучит из уст как владельцев «бэушных» автомобилей, самостоятельно занимающихся подкраской своих авто «на коленке», так и доверивших это дело гаражным или эстэошным профессионалам. Да что там, сам не без греха: в стародавние времена, когда я еще не занимался полной реставрацией «самобеглых колясок» и не вникал в природу возникновения коррозии, не раз задумывался над этим вопросом. Почему же автомобили, как и все сделанное из металла, ржавеют? Почему после окраски эта зараза зачастую вылезает снова и снова, что ты с ней ни делай? Народная мудрость на этот счет гласит: «Ржавчина — раковая болезнь металла, если появилась — будет расползаться, хоть ты лопни» («О’кей Google!»).
В свое время, не найдя готового ответа как на просторах Интернета, так и у знакомых автомаляров, пришлось начать с теоретических азов. Проведя ряд экспериментов по консервации коррозии с последующим наблюдением за «пациентами», могу дать доступное объяснение данного процесса и методы борьбы с ним.
«Коррозия, ржавление, ржа — это самопроизвольное разрушение металлов в результате химического или физико-химического взаимодействия с окружающей средой».
Схематически ее изображают следующим образом:
Говоря человеческим языком, молекулы железа, взаимодействуя с молекулами кислорода и воды, дают на выходе гидроксид железа Fe(OH)3 (ржавчину).
Что же, с вопросом «кто виноват?» все ясно, теперь осталось понять «что делать?».
Ответ: единственный способ обезопаситься от ржи на долгосрочный период — это провести комплекс мероприятий, направленных на удаление собственно коррозии (ржавчины) с последующей консервацией пораженного места от воздействия кислорода и воды.
1. Нужно устранить ржавчину механическим методом.
а) Пескоструйная обработка.
От себя скажу, что для локальной зачистки небольших «жуков» вполне подойдет бытовой компрессор на 220 В с пескоструйными «пистолетиками» за 400.000-500.000 бел. рублей.
Замечу, что полноценную пескоструйную зачистку соорудить в гаражных условиях без наличия 380 В практически нереально.
б) Механический метод. Для этого идеально подходят виниловые насадки типа 3M Scotch-Brite Clean’n’Strip™ и их бюджетные аналоги.
Насадки существуют в вариантах крепления на «болгарку» и на дрель (с помощью нехитрого переходника, который в народе заменяет болт, гайка и пара шайб) и буквально «выгрызают» коррозию из целого металла. Применять для такой работы металлические «ерши» и «чашки» категорически нельзя! Несмотря на красивый блестящий металл, оставляемый после их работы, по сути, происходит «зализывание» коррозии целым металлом. Обработанное «ершом» место достаточно потереть «наждачкой», чтобы убедиться в правоте моих слов, — из-под блестящего металла покажутся рыжие точки.
Независимо от выбранного вами метода зачистки пораженное место нужно контрольно обработать химическим методом (преобразователем ржавчины) с (внимание. ) обязательным последующим смывом преобразователя раствором воды с содой. Только таким образом можно нейтрализовать кислоту, содержащуюся в преобразователе. Не сделаете этого, и при дальнейшем попадании на это место воды оставшаяся кислота начнет «пожирать» целый металл.
Лично я предпочитаю удалять ржавчину не физическим, а электрохимическим методом.
в) «О’кей Google», еще раз покажи «как работает электрохимический метод удаления коррозии»
Вкратце: в воду засыпается небольшое количество кальцинированной соды (продается в хозяйственных магазинах), опускается зачищаемая деталь и электрод (ненужный кусок металла). После на очищаемую деталь подается минус 12 вольт, на электрод — плюс 12 вольт, и в зависимости от силы тока (в качестве источника питания удобно брать старый блок питания от компьютера) и площади детали и электрода через 1-12 часов вся ржавчина практически волшебным образом переходит на электрод. Остается лишь вымыть зачищаемую деталь и зачистить ее от следов бывшей ржавчины хотя бы железной щеткой.
Применение данного метода, по сути, ограничивается объемом применяемой емкости для опускания детали и наличием места для установки данной емкости.
И если, скажем, тормозной суппорт можно зачистить в пластиковом ведре, установленном на балконе квартиры, то для зачистки двери или капота вам понадобится емкость наподобие «еврокуба».
Увы, даже при этом полная зачистка кузова останется лишь в мечтах. Хотя я знаю случаи, когда импровизированную «ванну» делали на даче из обрешетки и баннерной ткани и производили полноценную зачистку демонтированной рамы внедорожника.
2. При наличии нескольких очагов коррозии нужно снять все покрытие с элемента. Да-да, как это ни прискорбно, но если вы хотите обезопасить свой 10-15-летний автомобиль от коррозии или продлить жизнь ремонтному покрытию, нужно зачистить хотя бы некоторую часть кузовного элемента, а далее сделать выводы.
Под краской зачастую «живет» уже множество нарождающихся «жуков», которые через сезон-два заявят о своем существовании.
3. Далее все работы с поверхностью (после первоначальной мойки или мойки после электрохимического метода) следует проводить без воды. Это делается во избежание контакта влаги с зачищенным металлом или (что наиболее опасно) задержки части влаги в наносимых слоях материала. Ведь еще из школьного курса известно, что влага при замерзании расширяется, оставшаяся под грунтом или в толще шпатлевки вода может не только вызвать коррозию, но и, замерзнув, образовать в покрытии микротрещину с последующим прямым доступом воды и кислорода к столь драгоценно защищаемой нами поверхности
4. И самый важный пункт — чем защитить металл после зачистки от повторного ржавления или хотя бы замедлить данный процесс, растянув его на годы. Для этого существует специальный антикоррозионный эпоксидный грунт.
Запомните: только эпоксидная смола не пропускает через себя молекулярную воду. Все другие типы покрытия (акриловый грунт, который, по сути, является только порозаполнителем, предназначен для выравнивания поверхности и никакой антикоррозионной роли не играет, акриловая краска, базовая краска, лак и т.д.) в различной степени пропускают молекулы воды.
По сути, все лакокрасочные материалы (ЛКМ) для воды являются аналогом москитной сетки, только ячейки-поры у всех типов покрытия разной величины. У эпоксидной смолы эти ячейки имеют наименьший размер.
Если обобщить перечисленные 4 пункта, то можно понять технологию защиты кузова автомобиля как целиком, так и от локальных «жуков», что может в различных вариациях подойти как обычному автовладельцу, думающему, как убрать «жук» с арки, так и окрасочному автосервису, желающему дать гарантию на свою работу не на стандартные 6 месяцев, а на 3-4 года и более!
Технология для автосервисов (для 10-летних авто и старше): голый, зачищенный по технологии металл — акриловый грунт — шпатлевание — затирка — акриловый грунт и проявка грунта — исправление огрехов шпатлевания — эпоксидный грунт и акриловый грунт (технология «мокрый по мокрому») — предокрасочная затирка (если красим не «мокрый по мокрому») — окраска.
Технология для обычного автовладельца: затираем «жука» виниловым кругом на дрели, обрабатываем преобразователем ржавчины, смываем преобразователь водой с добавлением соды — сушим — затираем «наждачкой» — наносим слой эпоксидной смолы — окрашиваем в цвет авто хотя бы кисточкой.
Вариации между двумя этими вариантами каждый может делать исходя из своих технических возможностей.
При всей простоте предложенного метода я чуть не забыл поделиться с вами маленьким но. Знаете, это как в анекдоте про то, чем китайская копия отличается от оригинала: по сути, копия и выглядит точно так же, как оригинал, и устроена подобно ему, но китайская копия не работает как оригинал.
Так и тут: любая более-менее глубокая коррозия, разрушая металл, образует в его толще микропоры, по которым может «питаться» кислородом и влагой с обратной стороны кузовного металла, так что, обрабатывая одну сторону «жука», не забудьте о второй стороне! К сожалению, не всегда к ней можно получить доступ, но хотя бы проантикорить ремонтные места с обратной стороны необходимо, однако это уже совсем другая история!
Если вы считаете, что на поставленный вопрос дан подробный ответ, предлагаю высказаться в комментариях, а также рассказать, как лично вы боролись с коррозией и чем эта борьба закончилась.
P.S. Надеюсь, теперь вы понимаете причину, почему на покрашенных кусках в первую же зиму ржа из-под краски лезет, почему большинство покрасочных сервисов предпочитает давать гарантию на свои работы на 6 месяцев? От себя добавлю, что сделанные по данной технологи даже «пожилые» советские автомобили спустя 3-4 года и более после окраски сохраняют внешний вид с полным отсутствием коррозии (при условии своевременной ликвидации сколов покрытия), собственно моя «Волга» тому живой пример.
Сергей ЖИЛЬЦОВ
Фото из архива автора и открытых источников
Материал опубликован в рамках Конкурса читательских материалов, рубрика — «По локоть в масле». Главный приз за лучший материал — сертификат на 6.000.000 рублей на покупку любых шин в любом магазине компании «Автосеть» . А вторы самых интересных материалов получат предложение поработать в ABW.BY!
Ознакомиться со всеми подробностями участия и полным списком призов можно по ссылке. Напоминаем, что прием работ уже окончен. Мы получили на порядок больше материалов, чем рассчитывали, а потому продолжим публиковать работы до конца января, после чего подведем итоги конкурса.
Найти оригинальные кузовные запчасти б/у вы можете, воспользовавшись поиском сайта-агрегатора BAMPER.BY. Здесь собрано более 287.000 предложений от различных продавцов с фотографиями и ценой каждой детали. Поиск любой запчасти — в три клика.
Генеральный партнер конкурса:
Сеть торгово-сервисных шинных центров «Автосеть»
Партнеры рубрики «Маршрут мечты»:
Магазин автомобильных запчастей и аксессуаров «Территория тюнинга»
Официальный импортер Volkswagen в Беларуси СООО «Атлант-М Фарцойгхандель»
Тема: «Коррозия металлов и меры борьбы с ней». Занятие 1.
Как организовать дистанционное обучение во время карантина?
Помогает проект «Инфоурок»
ЦК КТЭЛА
Раздел I . ФИЗИКО-ХИМИЧЕСКИЕ ОСНОВЫ МАТЕРИАЛОВЕДЕНИЯ
Тема 1.8. Коррозия металлов и меры борьбы с ней.
1. Общие сведения о коррозии металлов. Влияние коррозии на надежность АТ и экономику
2. Виды коррозии: химическая и электрохимическая коррозия
3. Факторы влияющие на образование коррозии
4. Формы коррозионных разрушений
1. Общие сведения о коррозии металлов. Влияние коррозии на надежность АТ и экономику
Коррозией называется разрушение металлов и некоторых других твердых тел, вызываемое химическими и электрохимическими процессами.
Существенное влияние на коррозию оказывают среды. Однако степень коррозионного разрушения зависит и от многих других факторов. Наиболее существенными из них являются состав и состояние поверхности металла, состав самой коррозионной среды и лекальные условия.
Коррозионное разрушение может происходить под действием горячих и раскаленных газов. Примером газовой коррозии может быть окисление лопаток турбины, соплового аппарата реактивных двигателей, прогорание клапанов, камер сгорания и других деталей, работающих при высоких температурах.
Многие детали самолетов подвергаются коррозии в жидкостных средах — морской и речной воде, топливе и масле. Разрушение в этом случае происходит под действием жидкостной коррозии.
Значительное количество авиационных деталей подвергается воздействию атмосферной коррозии (обшивка крыльев, фюзеляжа, оперения и др.).
Коррозия приводит к уменьшению прочности деталей, особенно тонкостенных деталей. Коррозия наружных поверхностей самолета приводит к ухудшению его обтекаемости. Ежегодные потери металла от коррозии исчисляются миллионами тонн.
Борьбе с коррозией в авиации уделяется особое внимание.
2. Виды коррозии: химическая и электрохимическая коррозия
Классифицировать коррозию принято по механизму, условиям протекания процесса и характеру разрушения (см. рис. 1.1).
По механизму протекания коррозионные процессы, согласно ГОСТ 5272 — 68, подразделяются на два типа: электрохимические и химические .
К электрохимической коррозии относят процесс взаимодействия металла с коррозионной средой, при котором ионизация атомов металла и восстановление окислительных агентов среды протекают не в одном акте и зависят от электронного потенциала (наличия проводников второго рода). Рассмотрим несколько видов электрохимической коррозии:
1) атмосферная — характеризует процесс в условиях влажной воздушной среды. Это наиболее распространенный вид коррозии, так как большинство конструкций эксплуатируют в атмосферных условиях. Ее можно разделить следующим образом: на открытом воздухе, с возможностью попадания на поверхность машин осадков, или с защитой от них в условиях ограниченного доступа воздуха и в замкнутом воздушном пространстве;
Рис. 1.1. Классификация коррозии
2) подземная — разрушение металла в почвах и грунтах. Разновидность этой коррозии — электрохимическая коррозия под воздействием блуждающих токов. Последние возникают в грунте вблизи источников электрического тока (систем передачи электроэнергии, электрифицированных транспортных путей);
3) жидкостная коррозия , или коррозия в электролитах . Ее частным случаем является подводная коррозия — разрушение металлических конструкций, погруженных в воду. По условиям эксплуатации металлоконструкций, этот вид подразделяют на коррозию при полном и неполном погружении; при неполном погружении рассмотрен процесс коррозии по ватерлинии. Водные среды могут отличаться коррозийной активностью в зависимости от природы растворенных в них веществ (морская, речная вода, кислотные и щелочные растворы химической промышленности и т. п.). При подводной коррозии возможны процессы коррозии оборудования в неводных жидких средах, которые подразделяют на неэлектропроводящие и электропроводящие. Такие среды специфичны для химической, нефтехимической и других отраслей промышленности. К химической коррозии относят процесс, в котором окисление металла и восстановление среды представляют единый акт (отсутствие проводников второго рода).
Химическая коррозия — это разрушение металлов в окислительных средах при высоких температурах. Различают два вида: газовая (т. е. окисление металла при нагреве) и коррозия в неэлектролитах :
а) характерной особенностью газовой коррозии является отсутствие влаги на поверхности металла. На скорость газовой коррозии влияет, прежде всего температура и состав газовой среды. В промышленности часто встречаются случаи этой коррозии: от разрушения деталей нагревательных печей до коррозии металла при термической обработке.
б) коррозия металлов в неэлектролитах, независимо от их природы, сводится к химической реакции между металлом и веществом. В качестве неэлектролитов используют органические жидкости.
В особую группу следует выделить виды коррозии в условиях воздействия механических напряжений ( механическая коррозия ). Эта группа включает:
коррозию под напряжением , характеризуемую разрушением металла при одновременном воздействии коррозионной среды и постоянных или переменных механических напряжений;
коррозионное растрескивание — при одновременном воздействии коррозионной среды и внешних или внутренних механических напряжений растяжения с образованием транскристаллитных трещин.
Различают самостоятельные виды коррозии:
1) коррозия при трении — разрушение металла, вызываемое одновременным воздействием коррозионной среды и трения;
2) фреттинг-коррозия — разрушение при колебательном перемещении двух поверхностей относительно друг друга в условиях воздействия коррозионной среды;
3) коррозионная кавитация — разрушение при ударном воздействии среды;
4) коррозионная эрозия — при истирающем воздействии среды;
5) контактная коррозия — разрушение одного из двух металлов, находящихся в контакте и имеющих разные потенциалы в данном электролите.
Следует различать коррозию и эрозию.
Эрозия от латинского слова erodere (разрушать) — постепенное механическое разрушение металла, например при истирании трущихся частей механизмов.
Самостоятельный вид коррозии — биокоррозия — это разрушение металла, при котором в качестве значимого выступает биофактор. Биоагенты — микроорганизмы (грибы, бактерии), которые являются инициаторами или стимуляторами процесса коррозии.
По характеру разрушения коррозия делится на сплошную (или общую) и местную (локальную). Сплошная коррозия охватывает всю поверхность металла, при этом она может быть равномерной или неравномерной. Местная коррозия происходит с разрушением отдельных участков поверхности металлов. Разновидность этой коррозии: точечная (питтинг), коррозия пятнами и сквозная коррозия.
Подповерхностная коррозия начинается с поверхности, но развивается преимущественно под ней таким образом, что продукты коррозии сосредоточены внутри металла. Ее разновидность — послойная коррозия , распространяющаяся преимущественно в направлении пластической деформации металла.
Структурная коррозия связана со структурной неоднородностью металла. Ее разновидность — межкристаллитная — разрушение металла по границам кристаллитов (зерен) металла; внутрикристаллитная — разрушение металла по зернам кристаллитов. Наблюдается при коррозийном растрескивании, протекающем под влиянием внешних механических нагрузок или внутренних напряжений.
Ножевая коррозия — локализованное разрушение металла в зоне сплавления сварных соединений в жидких средах с высокой коррозионной активностью.
Щелевая коррозия — усиление процесса разрушения металла в зазорах между двумя металлами.
Избирательная коррозия — разрушение одной структурной составляющей или одного компонента металла в высокоактивных средах. Существует ряд разновидностей: графитизация чугуна (растворение ферритных или перлитных составляющих) и обесцинкование (растворение цинковой составляющей) латуней.
3. Факторы влияющие на образование коррозии
Факторы, влияющие на возникновение коррозии, можно разделить на внутренние и внешние .
К внутренним факторам относятся: состав, строение, механическая напряженность и состояние поверхности.
Состав сплава оказывает наиболее существенное влияние на развитие коррозии. К коррозионностойким металлам относятся металлы, обладающие положительными значениями электродных потенциалов (медь, золото, платина и др.).
Высокой коррозионной стойкостью обладают также металлы, способные при окислении образовывать защитные оксидные пленки (хром, никель). Магний и его сплавы не образуют на поверхности защитные оксидные пленки, поэтому они не обладают коррозионной стойкостью. Кроме того, магниевые сплавы обладают очень низким значением электродного потенциала. Алюминий также обладает высокой коррозионной стойкостью, так как на его поверхности образуется защитная оксидная пленка.
На развитие коррозии значительное влияние оказывает чистота сплавов . Всякого рода загрязнения, оставшиеся после технологической обработки, например флюсы, поглащают влагу и создают коррозионную среду. Флюсы могут оставаться после сварки, поэтому после сварки детали необходимо тщательно очищать.
Существенное влияние на развитие коррозии оказывают внутренние напряжения , оставшиеся в металле после термической или механической обработки. При увеличении внутренних напряжений потенциал сплава становится более отрицательным, приводит к электрохимическому разрушению наиболее нагруженных участков. Пластическая деформация способствует развитию коррозии вследствие образования межкристаллитных микропор и проникновения в них влаги.
Если на деталь одновременно действует коррозионная среда и знакопеременная нагрузка, то происходит разрушение, которое принято называть коррозионной усталостью . Это явление происходит вследствие образования и развития трещин, идущих от поверхности вглубь. Коррозионная среда, проникая в эти трещины, облегчает разрушение. В этих условиях разрушение может происходить при напряжениях, меньших предела усталости.
К внешним факторам , влияющим на развитие коррозии, относится среда, в которой корродирует металл (водная среда, температура). Большое значение имеет концентрация ионов водорода. Кислые среды опасны для таких металлов, как магний, алюминий, железо, цинк. Алюминий и цинк легко разрушаются в щелочных средах. Опасной коррозионной средой для авиационных сплавов является морская вода.
Большое влияние на процесс коррозии в водных средах оказывает растворенный в воде кислород. Кислород окисляет металл. Появление оксидной пленки делает потенциал металла более положительным. Интенсивность коррозии при этом уменьшается. Установлено, что в водных средах наиболее опасными являются те участки, куда доступ кислорода затруднен (клепочные швы и др.).
На коррозионное разрушение поверхности самолета большое влияние оказывают такие факторы, как влажность, загрязнение воздуха пылью и газами. Влага способствует развитию электрохимической коррозии, так как содержит различные растворенные газы — СО 2 , SO 2 , окислы азота, соли и др. Осевшая на поверхности самолета пыль , которая будучи гигроскопичной, притягивает влагу, также способствует развитию очагов коррозии. На абсолютно чистой поверхности в меньшей степени конденсируется влага, чем на пыльной.
На развитие атмосферной коррозии оказывает влияние состав газов . Особенно вредными являются сернистый газ SO 2 , сероводород H 2 S и хлористый водород HCl . Резкий перепад температур также оказывает влияние на возникновение коррозии. При возвращении самолета из высотного полета холодные детали отпотевают, на них конденсируется влага и создаются предпосылки развития электрохимического процесса.
Коррозию самолетных деталей могут вызвать жидкости гидросистемы, кислоты, щелочи. Очень сильно поражает алюминиевые сплавы аккумуляторная щелочь.
4. Формы коррозионных разрушений
Коррозия, в зависимости от природы металла, агрессивной среды и других условий, приводит к различным видам разрушений. На рисунке 1.2 представлены разрезы через прокорродировавший образец металла, показывающие возможные изменения рельефа поверхности в результате коррозии.
Виды коррозии металла и борьба с ней
Коррозия металла является широко распространенной причиной, приводящей в негодность различные детали из металла. Коррозией металла (или ржавлением) называют разрушение металла под воздействием физических и химических факторов. К факторам, вызывающим коррозию, относят природные осадки, воду, температуру, воздух, различные щелочи и кислоты и т.д.
1 Разновидности ржавления
Коррозия металла становится серьезной проблемой при строительстве, в быту и на производствах. Чаще всего конструкторы предусматривают защиту металлических поверхностей от ржавчины, но иногда ржавление происходит на незащищенных поверхностях и на специально обработанных деталях.
Металлические сплавы лежат в основе жизнедеятельности человека, они окружают его практически везде: в быту, на работе, в процессе отдыха. Не всегда люди замечают металлические вещи и детали, но они постоянно им сопутствуют. Различные сплавы и чистые металлы являются самыми производимыми веществами на нашей планете. Современная промышленность выпускает различные сплавы в 20 раз больше (по массе), чем все остальные материалы. Несмотря на то что металлы считаются одними из наиболее прочных веществ на Земле, они могут разрушаться и терять свои характеристики в результате процессов ржавления. Под воздействием воды, воздуха и других факторов происходит процесс окисления металлов, который и называют коррозией. Несмотря на то что корродировать может не только металл, но и каменные породы, ниже будут рассмотрены процессы, связанные именно с металлами. Здесь стоит обратить внимание на то, что некоторые сплавы или металлы больше подвержены коррозии, чем другие. Это обусловлено скоростью протекания процесса окисления.
Самое распространенное вещество в сплавах — это железо. Коррозия железа описывается следующим химическим уравнением: 3O2+2H2O+4Fe=2Fe2O3. H2O. Полученный в результате оксид железа и является той рыжей ржавчиной, портящей предметы. Но рассмотрим виды коррозии:
- Водородная коррозия. На металлических поверхностях практически не встречается (хотя теоретически возможна). В связи с этим описываться не будет.
- Кислородная коррозия. Аналогична водородной.
- Химическая. Реакция происходит из-за воздействия металла с каким-либо фактором (например, воздухом 3O2+4Fe=2Fe2O3) и протекает без образования электрохимических процессов. Так, после воздействия кислорода с поверхностью появляется оксидная пленка. На некоторых металлах такая пленка достаточно прочна и не только защищает элемент от разрушительных процессов, но и повышает его прочность (например, алюминий или цинк). На некоторых металлах такая пленка очень быстро отслаивается (разрушается), например, у натрия или калия. А большинство металлов разрушаются достаточно медленно (железо, чугун и т.д.). Так, например, происходит коррозия чугуна. Более часто ржавление происходит при контакте сплава с серой, кислородом, хлором. Из-за химической коррозии ржавеют сопла, арматура и т.д.
- Электрохимическая коррозия железа. Данный вид ржавления происходит в средах, которые проводят электричество (проводники). Время разрушения различных материалов при электрохимических реакциях разное. Электрохимические реакции наблюдаются в случаях контакта металлов, которые находятся на расстоянии в ряду напряженности. Например, изделие изготовленное из стали, имеет медные напайки/крепления. При попадании воды на соединения медные части будут катодами, а сталь — анодом (каждая точка имеет свой электрический потенциал). Скорость протекания таких процессов зависит от количества и состава электролита. Для протекания реакций нужно наличие 2 разных металлов и электропроводящей среды. При этом разрушение сплавов прямо пропорционально зависит от силы тока. Чем больше ток, тем быстрее реакция, чем быстрее реакция, тем быстрее разрушение. В некоторых случаях катодами служат примеси сплава.
Также стоит отметить подвиды, которые бывают при ржавлении (описывать не будем, только перечислим): подземная, атмосферная, газовая, при разных видах погружения, сплошная, контактная, вызываемая трением и т.д. Все подвиды можно отнести к химическому или электрохимическому ржавлению.
2 Что наиболее часто ржавеет и как от этого предохраняться
При строительстве часто встречается коррозия арматуры и сварных конструкций. Коррозия часто происходит из-за несоблюдения правил хранения материала или невыполнения работ по обработке прутьев. Коррозия арматуры довольно опасна, поскольку арматуру закладывают для усиления конструкций, и в результате разрушения прутьев возможен обвал. Коррозия сварных швов не менее опасно, чем коррозия арматуры. Это также значительно ослабит шов и может привести к разрыву. Есть достаточно много примеров, когда ржавчина на силовых конструкциях приводит к обрушению помещений.
Другие часто встречающиеся в быту случаи ржавления — порча бытовых орудий труда (ножей, столовых приборов, инструмента), порча металлоконструкций, порча средств передвижения (как наземных, так и воздушных и водных) и т.д.
Пожалуй, самые часто встречающиеся ржавые вещи — это ключи, ножи и инструменты. Все эти предметы подвергаются ржавлению из-за того, что трением снимается защитное покрытие, которое оголяет основу.
Основа подвергается процессам разрушения из-за контактов с агрессивными средами (особенно ножи и инструменты).
Кстати, разрушения вещей, которые часто используются в быту, можно наблюдать практически повсеместно и регулярно, в то же время некоторые металлические предметы или конструкции могут простоять ржавыми десятилетия и будут исправно выполнять свои функции. Например, ножовка, которой часто пилили бревна и оставили на месяц в сарае, быстро проржавеет и может сломаться в процессе работы, а столб с дорожным знаком может простоять десять, а то и более лет ржавым и не разрушится.
Поэтому все металлические вещи следует защищать от коррозии. Методов защиты несколько, но все это химия. Выбор такой защиты зависит от типа поверхности и действующего на нее разрушительного фактора.
Для этого поверхность тщательно очищают от грязи и пыли, для того чтобы исключить возможность непопадания защитного покрытия на поверхность. Затем ее обезжиривают (для некоторых типов сплава или металла и для некоторых защитных покрытий это является необходимым), после чего наносят защитный слой. Наиболее часто защиту обеспечивают лакокрасочные материалы. В зависимости от металла и факторов используются разные лаки, краски и грунты.
Другой вариант — нанесение тонкого защитного слоя из другого материала. Обычно этот способ практикуется на производстве (например, оцинковка). В итоге потребителю практически ничего не требуется делать после приобретения вещи.
Другой вариант — создание специальных сплавов, которые не окисляются (например, нержавейка), однако они не гарантируют 100% защиты, более того, некоторые вещи из таких материалов окисляются.
Важными параметрами защитных слоев являются толщина, срок службы и скорость разрушения под активным неблагоприятным воздействием. При нанесении защитного покрытия крайне важно точно вписаться в допустимую толщину слоя. Обычно производители лакокрасочных материалов указывают его на упаковке. Так, если слой будет больше максимально допустимого, то это вызовет перерасход лака (краски), и слой может разрушаться под сильным механическим воздействием, более тонкий слой может стираться и сократить срок защиты основы.
Правильно выбранный защитный материал и правильно нанесенный на поверхность гарантирует на 80% то, что деталь не будет подвержена коррозии.
3 Что делать, если ржавчина уже есть
Многие люди в быту не задумываются над тем, как защитить свои вещи ото ржи. И получают проблему в виде испорченного предмета. Как правильно решить эту проблему?
Для того чтобы произвести восстановление вещи или детали от ржавчины, первым делом следует снять весь рыжий налет до чистой поверхности. Он снимается с помощью наждачной бумаги, напильников, сильными реагентами (кислотами или щелочами), но особую славу в этом заслужили напитки типа «Кока-Колы». Для этого вещь погружают полностью в емкость с чудо-жидкостью и оставляют на некоторое время (от нескольких часов до нескольких суток — время зависит от вещи и поврежденной площади).
После того как поверхность очищена, выполняются абсолютно все процедуры по защите от коррозии. То есть на поверхность наносят защитные лакокрасочные покрытия, напыления или хромируют. Главное во всей процедуре — это полностью очистить поврежденное место от ржавчины.
4 Почему надо бороться со ржавчиной
Многие люди часто не обращают внимание на рыжие пятна и на испорченные вещи. Ими продолжают работать, а после окончательного разрушения приобретают новые. На самом деле это дополнительные траты бюджета, в данном случае семейного.
Согласно данным ООН, каждая страна в год теряет от 0,5 до 7-8% валового национального продукта из-за коррозии. Парадокс заключается в том, что менее развитые страны теряют меньше, чем развитые. А 30% всех выпускаемых стальных изделий на планете идет на замену проржавевшим. Поэтому настоятельно рекомендуется отнестись к этой проблеме серьезно.
Заказ звонка
Козырьки и навесы, произведенные нами, служат надежной защитой от дождя, снега и прямых солнечных лучей. Покрытием для навеса служат листы сотового или монолитного поликарбоната, из-за своей прочности получившего название «металлическое стекло». Сталь, из которой изготовлены каркасы, не подвержена воздействию окружающей среды в виде влаги и выхлопов, что особо ценно.
Эксклюзивные лестницы, разработанные специалистами нашей компании, украсят собой любой, самый изысканный особняк, офис преуспевающей компании, квартиру с дизайнерским ремонтом. Мы спроектируем и изготовим любой тип изделий, будь это изящные винтовые лестницы, необычные лестницы на больцах, тетивах. Для профессионалов нашей компании не составит труда рассчитать.
Расчет, изготовление, монтаж металлоконструкции – непростой процесс. Малейшая ошибка здесь может обернуться большой трагедией. Специалисты нашей компании имеют огромный опыт в производстве ферм, стоек, опорных колонн и конструкций другого типа. Наше предприятие изготавливает изделия из качественного металла, что гарантирует прочность изделия любого уровня сложности.
Наша компания изготавливает надежные, современные ограждения соответствующие всем стандартам, предъявляемым к конструкциям такого типа. Мы проектируем, создаем, монтируем удобные ограждения для пандусов, прочные ограждения кровли, эксклюзивные уличные и придомовые ограждения. Сделанные из высококачественной нержавеющей и черной стали, они долговечны.
Оригинальные поручни и перила для лестниц, сконструированные мастерами по индивидуальным чертежам, заказчика, украсят собой любой коттедж, загородный дом, офис. Изготовленные из высококачественной нержавеющей и черной стали, они выдерживаю большие нагрузки и неподвержены влиянию окружающей среды. Перила, с напылением из нитрида титана блеском и прочность.
Как избавиться от коррозии на металлических конструкциях
Металлические поверхности и конструкции востребованы в строительной сфере благодаря своим высоким эксплуатационным характеристикам. В загородном строительстве металл используется при прокладке инженерных коммуникаций, возведении ограждений на участке и настила кровли, в городе его широко применяют для изготовления балконных и лестничных ограждений, оконных решеток, батарей отопления. Но, к сожалению, этот крепкий и долговечный материал имеет свою уязвимую сторону и каждому хотя бы раз приходилось решать проблему, как избавиться от коррозии.
Образование ржавчины на поверхности металла связано с химическими процессами его окисления под воздействием воздуха и влаги. В сухом помещении металлическая конструкция на протяжении долгого времени сохраняет свой исходный вид, поскольку отсутствует контакт металла и кислорода в присутствии влаги. Но стоит хотя бы капле воды попасть на металлическую поверхность, как начинается необратимый процесс окисления и разрушения.
Ржавчина не только ухудшает внешнюю привлекательность металлических конструкций, но и наносит непоправимый вред, стремительно разрушая структуру металла и тем самым снижая его прочность и надежность. Эксплуатация конструкций, «изъеденных» ржавчиной не безопасна и сопряжена с постоянным риском. Ведь если вовремя не остановить коррозию, то процесс окисления будет продолжаться до полного разъедания металлической конструкции или поверхности.
Существуют различные по эффекту способы борьбы с коррозией. Самый известный и распространенный метод, когда применяется механическая очистка металла от ржавчины. Для этого используются скребки, металлические щетки или болгарки с набором специальных дисков. Работа эта очень трудоемкая, долгая и не без последствий для металлических поверхностей, которые в результате механического воздействия покрываются царапинами и вмятинами. Но в запущенных случаях, когда пятна ржавчины стремительно разрастаются и процесс окисления заходит далеко, бороться с коррозией можно только радикально. Как, например, с использованием газовой горелки. Когда металлическую поверхность нагревают, а затем слой ржавчины удаляют жесткой щеткой или скребком.
Помимо появления дефектов на поверхности способ механической очистки от коррозийных пятен имеет и еще один недостаток – невысокую эффективность. При очистке часть ржавчины все равно остается на поверхности, и удалить ее можно только химическим путем. Многие рекомендуют использовать смесь из равных частей уксусной и лимонной кислот, вспоминая школьный курс химии и неустойчивость ржавчины перед сильными кислотными составами. Самостоятельно приготовленную кислотную смесь наносят на изъеденную ржавчиной поверхность и оставляют на пару часов, а затем поверхность хорошо отмывают с помощью проволочной щетки. Точно так же применяют насыщенный содовый раствор, разведя водой порошок натрия двууглекислого до состояния пасты.
Удаление ржавчины с металла можно провести и еще одним бытовым способом, который довольно хорошо знаком автомобилистам. Для него понадобится приготовить специальный раствор: к одной части парафина добавить девять частей керосина и выдержать состав сутки в герметично закупоренной посуде. Выдержанной смесью обмазывают поврежденные коррозией участки металла и оставляют на сутки. Практики утверждают, что по прошествии суток ржавчина легко и бесследно удаляется с металлической поверхности с помощью обычной мочалки или тряпки. Правда, весьма затруднительно представить антикоррозийную обработку этим способом, например, листовой кровли.
Как бы то ни было, чем думать, как бороться с коррозией и остановить ее распространение, проще и дешевле не допустить ее возникновения. Для этого металлические конструкции подвергают окрашиванию. Краска, нанесенная на металлическую поверхность, создает тонкую пленку, изолирующую металл от воздействия любых негативных атмосферных явлений. Одновременно с этим краска предохраняет металлические изделия от температурных воздействий и делает более привлекательным их внешний облик.
В состав таких красок по металлу входят преобразователи коррозии и активные химические компоненты, которые предотвращают процесс окисления. Антикоррозийная обработка металла специальными красками имеет много преимуществ, главное из которых, возможность обработать металлические поверхности любой конструкционной сложности и площади. Краска легко наносится и на декоративные ажурные решетки окон, и на ограждения приусадебной территории, и на сложную многощипцовую кровлю загородного дома.
Однако окраска металлических поверхностей полностью оправдает свое назначение только в том случае, если конструкция была тщательно к ней подготовлена. Другими словами, покрытие металлических поверхностей защитными антикоррозийными составами должны предварять работы по зачистке и обезжириванию конструкции с использованием уайт-спирита, нанесению ингибиторов коррозии и грунтовке. Грунт для обработки поверхности необходимо подбирать с учетом физико-химических свойств металлов. Но даже при грамотном подходе к работам по антикоррозийной обработке декоративно-защитное покрытие будет нуждаться в периодическом обновлении.
При покупке краски для антикоррозийной обработки обязательно нужно обратить внимание, для каких видов работ она предназначена: наружных или внутренних. По возможности желательно приобретать декоративно-защитные покрытия, на которых указана область применения. Покрытия для радиаторов отопления будут обладать необходимой стойкостью к воздействию высоких температур, а краска, предназначенная для металлической кровли, будет способна нейтрализовать негативное атмосферное воздействие, в том числе и кислотное.
Применение соответствующих покрытий гарантирует их полную эксплуатационную полезность. Другими словами, они надежно защищают металлические поверхности, металлические конструкции целиком от возникновения и распространения коррозии на протяжении всего срока, указанного производителем. До истечения этого времени покрытия не нуждаются в обновлении и применении дополнительных средств защиты. Главное, чтобы производитель краски по металлу вызывал доверие.
Читайте так же другие полезные статьи
Нержавеющая сталь – популярный материал, используемый для изготовления деталей, составляющих конструкций, например, панелей лифтовых кабин, витражных каркасов, заборов и ограждений, медицинских инструментов. Отличается повышенной прочностью, неизменностью характеристик при воздействии агрессивной среды или высокой температуры.
Лестницы на Больцах — самонесущие лесенки, ступени поддерживаются и соединяются друг с другом с помощью специальных токарных или литых элементов штампованных или выполненных.
Изделия из нержавеющей стали требуют, помимо прочностного расчета, качественное выполнение сварных соединении, потому при изготовлении металлоконструкций в частности ограждений из нержавеющей стали.
Покрытие нитрид титана — это соединение титана и азота, применяющееся в самых различных отраслях — от медицинской до машиностроения. В металлургии соединение встречается в качестве неметаллических добавок в сталях легированных титаном. Готовое вещество является порошком из мелких желтых и коричневых частиц. При напылении порошок приобретает золотистую окраску, которая может изменять яркость и глубину цвета.
Это незаменимый элемент, который связывает между собой разные уровни любого сооружения или дома. Трудно представить себе частный дом высотой более одного этажа или многоуровневую квартиру, где не было бы лестницы.
Что бы предотвратить неблагоприятные последствия пожаров и других катаклизмов, связанных, с экстренной эвакуацией людей необходимо тщательно просчитать лестницы эвакуационные наружные.
Русь издавна славилась искусными мастерами кузнечного дела и ковки металла, которые могут не только выковать сложнейшие изделия, но даже блоху подковать. Без преувеличения можно сказать, что художественная ковка — последнее «живое» ремесло в наше технократическое.
В экстерьере здания, сооружения важен каждый элемент. Неудивительно, что для создания долговечных входных групп, перил, ограждений, поручней применяют нержавеющую сталь, обладающую сильный устойчивостью к коррозии, прочностью. Материал гармонично сочетается.
В последнее время с развитием технологий производства изделий из металла металлоконструкций из нержавеющий стали широко расширились возможности предлагаемые заказчику в реализации его пожеланий и фантазий
Уже не один десяток лет в оформлении интерьеров используется самый изысканный и во многом недооцененный материал нержавеющая сталь. Это материал, который позволяет создать самые интересные и неожиданные образы и решения.