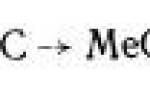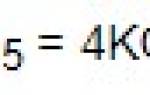Содержание
- Расчет температуры плавления и затвердевания стали
- Расчет температуры ликвидус стали
- При каких температурах плавятся различные металлы и неметаллы?
- Понятие о шкале температур
- Кристаллические решетки металла
- Температура плавления металлов
- Сплавы металлов
- Сплав Вуда
- Сплавы для пайки
- Температура плавления неметаллов
- Температура плавления стали
- Общее описание процесса
- Типы сплавов
- Жаропрочные стали и сплавы
- Свойства жаростойких и жаропрочных сплавов
- Классификация жаропрочных и жаростойких сплавов
- Стали по ГОСТ, классификация, свойства.
Температура плавки стали
Температура плавления (температура ликвидус) — это температура, при которой вещество переходит в полностью жидкое состояние. Температура затвердевания (температуру солидус) — это такая температура, при которой вещество переходит полностью в твердое состояние.
Для чистых веществ (элементов) температуры ликвидус и солидус совпадают. Для растворов же, к которым в том числе относятся сталь и чугун, существует, так называемый, температурный интервал кристаллизации, в котором одновременно сосуществуют твердая и жидкая фазы.
Расчет температуры плавления и затвердевания стали
Температуры плавления и затвердевания стали зависят от ее состава.
Как правило при расчете TL и TS делают допущение об аддитивности влиянии легирующих и примесей на значения этих величин. При этом изменение температуры плавления/затвердевания, обусловленное наличием того или иного элемента, рассчитывают как
TL/S сплав = Т — ΣdTL/Si
где TL/Sсплав — температура ликвидус / солидус сплава, К;
Т — температура плавления растворителя (железа), К;
dTL/Si — снижение TL и TS, обусловленное наличием в металле i-го элемента, К.
Влияние различных элементов на температуру плавления и кристаллизации определяют по диаграммам состояния для каждого элемента i (использованные диаграммы состояния приведены ниже в таблице).
При этом допускали, что их влияние на рассматриваемые величины носит линейный характер, т.е.
dTL/Si = kL/Si·[i]где kL/Si — средний коэффициент наклона линии ликвидус (солидус) на диаграмме состояния в определенном интервале концентраций рассматриваемого элемента, К/%;
[i] — концентрация элемента i, % масс.
kL/Si = <(TL/Si)а - (TL/Si)b>/<[i]а - [i]b>
где (TL/Si)а и (TL/Si)b — температура ликвидус/солидус расплава при концентрации элементаi в нем равной [i]а и [i]b, соответственно, К.
Конкретные значения kL/S i были получены следующим образом:
kLC = (1539 — 15. )/. = 64 kSC = (1539 — . )/. = 356 при С 0,1
kLCr = (1539 — 1515)/22 = 1,09 kSCr = (1539 — 1505)/22 = 1,54
kLNi = (1539 — 1449)/50 = 1,80 kSNi = (1539 — 1436)/50 = 2,06
kLMo = (1539 — 1460)/33 = 2,39 kSMo = (1539 — 1450)/33 = 2,70
kLV = (1539 — 1475)/30 = 2,13 kSV = (1539 — 1468)/30 = 2,37
kLS = (1539 — 1530)/0,20 = 45,0 kSS = (1539 — 1365)/0,20 = 870
если содержание серы более 0,2, то dTSS= 1539 — 1365 = 174
kLP = (1539 — 1400)/5 = 27,8 kSP = (1539 — 1050)/5 = 97,8
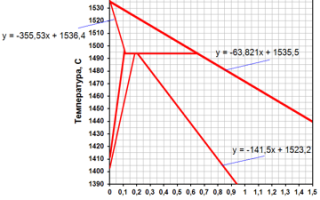
Влияние углерода на температуры ликвидус и солидус целесообразно рассчитывать с учетом изображенных на рисунке ниже рагрессионных выражений.
Таким образом, температура ликвидус и солидус рассчитываются как
Следует подчеркнуть, что величина TS не представляет практического интереса, так как в процессе кристаллизации происходит значимое перераспределение элементов между жидкой и твердой фазой, в результате которого жидкость обогащается ликватами, прежде всего углеродом, серой и фосфором (чем определяется способность элементов к ликвации Вы можете узнать здесь), что, естественно, снижает температуру затвердевания, поэтому температура, при которой разливаемый металл полностью затвердевает в большинстве случае составляет величину гораздо меньшую, чем расчетное значение TS.
Ниже приведена работа А. Н. Смирнова, более подробно рассматривающая вопрос определения температуры плавления и затвердевания стали
Расчет температуры ликвидус стали
А. Н. Смирнов, Л. Неделькович, М. Джурджевич, Т. В. Чернобаева и 3. Оданович
Донецкий государственный технический университет (Украина) и Белградский университет (Югославия)
Точная оперативная информация о температуре ликвидус стали имеет большое практическое значение, так как в зависимости от имеющегося в цехе оборудования для внепечной обработки именно эта температура определяет температурный режим от выпуска до окончания разливки плавки, особенно на МНЛЗ. Это дает возможность работать с оптимально низкой степенью перегрева и обеспечивает мелкозернистую литую структуру и высокое качество заготовки. Известно, что измерение температуры ликвидус (TL) не вызывает значительных затруднений. Однако заданный химический состав стали достигается к концу внепечной обработки перед началом непрерывной разливки, что существенно ограничивает возможности использования экспериментальных данных (записи кривой охлаждения). Поэтому для оперативного определения значения TL целесообразно проводить расчеты с использованием данных о химическом составе стали.
Между тем, выбор какого-либо универсального метода расчета температуры ликвидус на практике вызывает значительные затруднения, так как рекомендации специалистов, занимающихся решением этой проблемы, довольно противоречивы. Сравнение точности и надежности методов расчета TL для стали различных марок выполнено в настоящей работе.
Большая часть известных методов расчета температуры ликвидус углеродистой и легированной стали основана на полиномных выражениях, которые в обобщенном виде могут быть представлены следующим образом [1. 9]:
где Tплав Fe — температура плавления чистого железа (в соответствии с большей частью известных рекомендаций Tплав Fе = 1539 °С); а — коэффициент приведения температуры плавления чистого железа (вводится в случае принятия значения температуры плавления железа отличного от приведенного выше); а1 и а2 — коэффициенты значимости 1-го и 2-го порядка для соответствующего элемента i, содержащегося в стали данной марки; [i] — содержание элемента i в стали данной марки, %.
В качестве основы выражений такого типа принята гипотеза о том, что каждый из химических элементов влияет на снижение температуры ликвидус железа независимо один от другого. При этом результирующее влияние всех растворенных в стали элементов на снижение температуры ликвидус может быть получено на основании двойных диаграмм состояния Fe-Хi,. Поэтому эти выражения различаются только тем, каким образом аппроксимируется линия ликвидус в бинарной диаграмме со стороны железа. В простейшем случае она заменяется касательной прямой на линию ликвидус со стороны железа, а выражение для температуры ликвидус упрощается до полинома первого порядка. Подобные выражения, как видно из табл. 1 [1. 4], различаются по значениям коэффициентов аi и принятой температуре плавления железа.
Влияние изменения концентрации каждого химического элемента на снижение температуры плавления железа может быть также учтено описанием линии ликвидус с помощью полинома второго порядка или вписыванием ломаной линии в кривую значений температуры ликвидус. Причем неодинаковый наклон звеньев ломаной линии в концентрационных промежутках учитывает влияние собственной концентрации каждого элемента на снижение температуры плавления железа. В качестве иллюстрации в табл. 1 приведены данные работ [5. 7], где учитывается только концентрационная зависимость влияния углерода, и работ [8, 9], где эта концентрационная зависимость выражается и для ряда других элементов в стали. Приведенными в табл. 1 данными можно пользоваться только в тех концентрационных областях, в которых при затвердевании образуется твердый раствор.
Однако средние квадратичные отклонения σ (табл. 1) не могут служить обобщенным критерием оценки достоверности и применимости каждой из формул, так как специалисты обычно используют несколько отличные в техническом исполнении методы и приборы для измерения температуры ликвидус стали. По-видимому, такая оценка должна проводиться для данных, которые получены в примерно одинаковых условиях при достаточно надежном измерении температуры ликвидус применительно к большому массиву марок стали.
В настоящей работе были отобраны результаты измерений температуры ликвидус для стали 87 марок по данным А.А. Howe [10]. Химический состав стали некоторые из этих марок и результаты измерений температуры ликвидус приведены в табл. 2. При этом для стали состава 1-10 температуру ликвидус определяли путем термического анализа образца массой 400 г, для стали состава 11-20 — одновременно путем термического и дифференциального термического анализа образца массой 40 г.
Было определено, что расчетные значения температуры ликвидус в большей части случаев превышают экспериментальные данные. С уменьшением температуры ликвидус, которое соответствует росту содержания углерода и легирующих элементов в стали, величина разброса расширяется.
Результаты оценки достоверности расчетов температуры ликвидус (табл. 3) показывают, что использование предложенных формул не отличается высокой степенью точности, так как даже наиболее точные из результатов расчетов имеют среднее квадратичное отклонение около ±2,5, соответствующее полосе разброса ±7,5 °С.
По мнению авторов настоящей статьи, такое отклонение расчетных данных от экспериментальных может быть вызвано в основном тем, что эти формулы не учитывают характер взаимодействия отдельных химических элементов при определенной их концентрации. Из работ [11-13] известно, что, если при наличии какого-либо другого элемента или с увеличением собственной концентрации коэффициент активности данного элемента изменяется, то и его влияние на TL стали должно соответственно изменяться.
Возрастание влияния коэффициента активности углерода с повышением его концентрации в стали проиллюстрировано на примере стали, содержащей 1,48 % С (табл. 4). При таком увеличении коэффициента активности углерода его действительное влияние на снижение температуры ликвидус, определенное экспериментально, оказывается значительно большим, чем это можно принять по результатам расчетов по известным формулам. Поэтому в большей части случаев расчетные значения TL заметно превышают экспериментальные. В противном случае, если сталь содержит элемент, снижающий активность углерода, и соответственно углерод уменьшает активность этого элемента в стали (Б, табл. 4, марганцовистая сталь), действительное снижение температуры ликвидус, определенное экспериментально, меньше, чем рассчитайное по формулам, не учитывающим взаимное влияние активностей, что выражается в положительном отклонении разностей между экспериментальными и расчетными значениями TL. Более сложный пример (В, табл. 4) для стали с высоким содержанием никеля иллюстрирует большие отклонения разностей между экспериментальными и расчетными значениями TL в положительную сторону практически по всем формулам, что, по-видимому, является следствием неадекватного описания линии ликвидус в бинарной системе Fe-Ni.
Следует отметить, что рассмотрены (табл. 4) только двухкомпонентные и трехкомпонентные системы, причину отклонения расчетных экспериментальных значений TL в которых можно достаточно аргументированно объяснить. Наибольший разброс отклонений значений TL наблюдается для легированной стали многокомпонентного состава, где взаимодействие между элементами более сложное. Следовательно, для стали такого состава отклонения, вызванные неадекватным учетом эффектов таких взаимодействий на снижение температуры ликвидус, менее предсказуемы.
Как видно из табл. 2, для группы углеродистой и низколегированной стали dTср имеет отрицательное значение и по абсолютному значению в каждом отдельном случае большеdTmin. В более 90 % случаев значения dTmin распределены по нормальному закону в интервале ± 2 °С около фактической температуры ликвидус, а около 70 % — в интервале ± 1 °С.
Таблица 1. Коэффициенты a, а1 и a2 характеризующие степень влияния содержащихся в стали химических элементов на снижение температуры ликвидус*
При каких температурах плавятся различные металлы и неметаллы?
Металлы обладают рядом оригинальных свойств, которые присущи только этим материалам. Существует температура плавления металлов, при которой кристаллическая решетка разрушается. Вещество сохраняет объем, но уже нельзя говорить о постоянстве формы.
В чистом виде отдельные металлы встречают крайне редко. На практике применяют сплавы. У них есть определенные отличия от чистых веществ. При образовании сложных соединений происходит объединение кристаллических решеток между собой. Поэтому у сплавов свойства могут заметно отличаться от составляющих элементов. Температура плавления уже не остается постоянной величиной, она зависит от концентрации входящих в сплав ингредиентов.
Понятие о шкале температур
Некоторые неметаллические предметы тоже обладают похожими свойствами. Самым распространённым является вода. Относительно свойств жидкости, занимающей господствующее положение на Земле, была разработана шкала температур. Реперными точками признаны температура изменения агрегатных состояний воды:
- Превращения из жидкости в твердое вещество и наоборот приняты за ноль градусов.
- Кипения (парообразования внутри жидкости) при нормальном атмосферном давлении (760 мм рт. ст.) принята за 100 ⁰С.
Кристаллические решетки металла
В идеальном виде принято считать, что металлам свойственна кубическая решетка (в реальном веществе могут быть изъяны). Между молекулами имеются равные расстояния по горизонтали и вертикали.
Твердое вещество характеризуется постоянством:
- формы, предмет сохраняет линейные размеры в разных условиях;
- объема, предмет не изменяет занимаемое количество вещества;
- массы, количество вещества, выраженное в граммах (килограммах, тоннах);
- плотности, в единице объема содержится постоянная масса.
При переходе в жидкое состояние, достигнув определенной температуры, кристаллические решетки разрушаются. Теперь нельзя говорить о постоянстве формы. Жидкость будет принимать ту форму, в какую ее зальют.
Когда происходит испарение, то постоянным остается только масса вещества. Газ займет весь объем, который будет ему предоставлен. Здесь нельзя утверждать, что плотность постоянная величина.
Когда соединяются жидкости, то возможны варианты:
- Жидкости полностью растворяются одна в другой, так себя ведут вода и спирт. Во всем объеме концентрация веществ будет одинаковой.
- Жидкости расслаиваются по плотности, соединение происходит только на границе раздела. Только временно можно получать механическую смесь. Перемешав разные по свойствам жидкости. Примером является масло и вода.
Образующиеся растворимые друг в друге вещества при застывании образуют кристаллические решетки нового типа. Определяют:
- Гелиоцентрированные кристаллические решетки, их еще называют объёмно-центрированными. В середине находится молекула одного вещества, а вокруг располагаются еще четыре молекулы другого. Принято называть подобные решетки рыхлыми, так как в них связь между молекулами металлов слабее.
- Гранецентрированные кристаллические решетки образуют соединения, в которых молекулы компонента располагаются на гранях. Металловеды называют подобные кристаллические сплавы плотными. В реальности плотность сплава может быть выше, чем у каждого из входящих в состав компонентов (алхимики средних веков искали варианты сплавов, при которых плотность будет соответствовать плотности золота).
Температура плавления металлов
Разные вещества имеют различную температуру плавления. Принято делить металлы на:
- Легкоплавкие – их достаточно нагревать до 600 ⁰С, чтобы получать вещество в жидком виде.
- Среднеплавкие металлы расплавляются в диапазоне температур 600…1600 ⁰С.
- Тугоплавкими называют металлы, которые могут расплавляться при температуре более 1600 ⁰С.
В таблице по возрастанию показаны легкоплавкие металлы. Здесь видно, что самым необычным металлом является ртуть (Hg). В обычных условиях она находится в жидком состоянии. Этот металл имеет самую низкую температуру плавления.
Таблица 1, температуры плавления и кипения легкоплавких металлов:
Таблица 2, температуры плавления и кипения среднеплавких металлов:
Таблица 3, температуры плавления и кипения тугоплавких металлов:
Чтобы вести процесс плавки используют разные устройства. Например, для выплавки чугуна применяют доменные печи. Для плавки цветных металлов производят внутренний нагрев с помощью токов высокой частоты.
В изложницах, изготовленных из неметаллических материалов, находятся цветные металлы в твердом состоянии. Вокруг них создают переменное магнитное поле СВЧ. В результате кристаллические решетки начинают расшатываться. Молекулы вещества приходят в движение, что вызывает разогрев внутри всей массы.
При необходимости плавки небольшого количества легкоплавких металлов используют муфельные печи. В них температура поднимается до 1000…1200 ⁰С, что достаточно для плавки цветных металлов.
Черные металлы расплавляют в конвекторах, мартенах и индукционных печах. Процесс идет с добавлением легирующих компонентов, улучшающих качество металла.
Сложнее всего проводить работу с тугоплавкими металлами. Проблема в том, что нужно использовать материалы, имеющие температуру более высокую, чем температура плавления самого металла. В настоящее время авиационная промышленность рассматривает использование в качестве конструкционного материала Титан (Ti). При высокой скорости полета в атмосфере происходит разогрев обшивки. Поэтому нужна замена алюминию и его сплавам (AL).
Сплавы металлов
Чтобы проектировать изделия из сплавов, сначала изучают их свойства. Для изучения в небольших емкостях расплавляют изучаемые металлы в разном соотношении между собой. По итогам строят графики.
Нижняя ось представляет концентрацию компонента А с компонентом В. По вертикали рассматривают температуру. Здесь отмечают значения максимальной температуры, когда весь металл находится в расплавленном состоянии.
При охлаждении один из компонентов начинает образовывать кристаллы. В жидком состоянии находится эвтектика – идеальное соединение металлов в сплаве.
Металловеды выделяют особое соотношение компонентов, при котором температура плавления минимальная. Когда составляют сплавы, то стараются подбирать количество используемых веществ, чтобы получать именно эвтектоидный сплав. Его механические свойства наилучшие из возможных. Кристаллические решетки образуют идеальные гранецентрированные положения атомов.
Изучают процесс кристаллизации путем исследования твердения образцов при охлаждении. Строят специальные графики, где наблюдают, как изменяется скорость охлаждения. Для разных сплавов имеются готовые диаграммы. Отмечая точки начала и конца кристаллизации, определяют состав сплава.
Сплав Вуда
В 1860 г. американский зубной техник Барнабас Вуд искал оптимальные соотношения компонентов, чтобы изготавливать зубы для клиентов при минимальных температурах плавления. Им был найден сплав, который имеет температуру плавления всего 60,2…68,5 ⁰С. Даже в горячей воде металл легко расплавляется. В него входят:
- олово — 12,5…12,7 %;
- свинец — 24,5…25,0 %;
- висмут — 49,5…50,3 %;
- кадмий — 12,5…12,7 %.
Сплавы для пайки
На практике многие сталкиваются с плавлением при пайке деталей. Если поверхности соединяемых материалов очищены от загрязнений и окислов, то их нетрудно спаять припоями. Принято делить припои на твердые и мягкие. Мягкие получили наибольшее распространение:
- ПОС-15 — 278…282 °C;
- ПОС-25 — 258…262 °C;
- ПОС-33 — 245…249 °C;
- ПОС-40 — 236…241 °C;
- ПОС-61 — 181…185 °C;
- ПОС-90 — 217…222 °C.
Их выпускают для предприятий, изготавливающих разные радиотехнические приборы.
Твердые припои на основе цинка, меди, серебра и висмута имеют более высокую температуру плавления:
- ПСр-10 — 825…835 °С;
- ПСр-12 — 780…790 °С;
- ПСр-25 — 760…770 °С;
- ПСр-45 — 715…721 °С;
- ПСр-65 — 738…743 °С;
- ПСр-70 — 778…783 °С;
- ПМЦ-36 — 823…828 °С;
- ПМЦ-42 — 830…837 °С;
- ПМЦ-51 — 867…884 °С.
Использование твердых припоев позволяет получать прочные соединения.
Внимание! Ср означает, что в составе припоя использовано серебро. Такие сплавы обладают минимальным электрическим сопротивлением.
Температура плавления неметаллов
Неметаллические материалы могут быть представлены в твердом и жидком виде. Неорганические вещества представлены в табл. 4.
Таблица 4, температура плавления неорганических неметаллов:
На практике для пользователей наибольший интерес представляют органические материалы: полиэтилен, полипропилен, воск, парафин и другие. Температура плавления некоторых веществ показана в табл. 5.
Таблица 5, температура плавления полимерных материалов:
Внимание! Под температурой стеклования понимают состояние, когда материал становится хрупким.
Видео: температура плавления известных металлов.
Температура плавления стали
Стальные соединения изготавливаются из железа и углерода. Добиться прочности, твердости и других требуемых качеств позволяет добавление в сплав никеля, хрома, молибдена и других дополнительных компонентов. Одним из таких качеств является температура плавления стали, при которой материал переходит из твердого состояния в жидкое.
Общее описание процесса
Чтобы понять, при какой температуре плавится сталь, нужно рассмотреть этот процесс более детально. Расплавление происходит при нагревании. Нагревать материал можно как снаружи, так и изнутри. Внешний нагрев осуществляется в термических печах. Для того чтобы расплавить сплав изнутри, используется резистивный нагрев. Принцип резистивного нагрева заключается в электросопротивлении, которым обладают любые материалы.
Вне зависимости от типа термического воздействия, в материалах происходят одинаковые изменения. За счет нагревания тепловые колебания молекул усиливаются, что приводит к структурным дефектам решетки. Такие изменения способствуют разрыву межатомных связей, в результате чего сплав переходит в жидкое состояние.
Типы сплавов
В зависимости от интенсивности нагрева, требуемого для перехода металла из одного состояния в другое, сплавы разделяют на несколько видов.
Легкоплавкие. Их обработка может производиться даже без специального оборудования. Температура плавления стали в градусах Цельсия составляет 600. К числу легкоплавких металлов относятся свинец, олово и цинк.
Особого внимания заслуживает ртуть, способная переходить в жидкое состояние при -39°С.
Среднеплавкие. Температура плавления сталей находится в пределах 600°С-1600°С. К этой категории относятся алюминий, медь, олово, некоторые виды нержавейки и различные сплавы с небольшим содержанием хрома. Среднеплавкие соединения получили наибольшее распространение в промышленности и в быту.
Тугоплавкие. Соединения, входящие в данную категорию, способны переходить из твердого состояния в жидкое при нагреве свыше 1600°С. Это высоколегированные металлы, в состав которых входят вольфрам, титан и хром. Благодаря этим добавкам металл приобретает повышенную прочность, устойчивость к коррозии и химическим воздействиям. В частности, к тугоплавким сплавам относится нержавейка.
При наиболее низких температурных показателях плавятся щелочные металлы. Соответственно, для перехода в жидкое состояние не щелочных металлов температурный диапазон значительно увеличивается.
Градус кипения
В процессе нагрева материала важно не достичь его кипения, при котором из жидкого состояния он переходит в газообразное. Поэтому градус кипения является не менее важным технологическим показателем.
Градус кипения, как правило, вдвое выше градуса, при котором материалы расплавляются, и определяется при нормальном атмосферном давлении. При увеличении давления увеличивается и интенсивность нагрева. При уменьшении давления показатели уменьшаются.
Особенности углеродистой стали
Углеродистые соединения являются основным видом продукции, производимой на металлургических комбинатах. Кроме железа, в их состав входит углерод. Его концентрация не должна превышать 2,14%. В них присутствует небольшое количество примесей и легирующих компонентов в виде марганца, кремния и магния. Такие добавки позволяют улучшить их физические и химические показатели.
В зависимости от концентрации углерода углеродистые соединения делятся на следующие виды:
- низкоуглеродистые (содержание углерода не превышает 0,29%);
- среднеуглеродистые (до 0,6%);
- высокоуглеродистые (более 0,6%).
Углеродистые соединения используются в различных промышленных отраслях. В зависимости от сферы применения в них добавляются легирующие компоненты, позволяющие достичь специфических свойств, включая жаропрочность, коррозийную стойкость и пр. По этим критериям они подразделяются на следующие категории:
В инструментальные добавляется марганец, позволяющий значительно повысить качество металла. Температура плавления углеродистой стали составляет 1535°С.
Особенности легированной стали
В состав легированных соединений вводят дополнительные компоненты. В определенных количествах они придают им требуемые свойства. В зависимости от концентрации таких элементов они подразделяются на следующие виды:
- низколегированные (с концентрацией 2,5%);
- среднелегированные (до 10%);
- высоколегированные (свыше 10%).
За счет добавления дополнительных компонентов удается повысить прочность, коррозийную стойкость и улучшить другие характеристики. В качестве легирующих компонентов выступают хром, медь, никель, азот, ванадий и пр. Температура плавления легированной стали колеблется в пределах 1400°С-1480°С.
Особенности нержавейки
Нержавейка – это сплав, устойчивый к сухой и влажной коррозии, и невосприимчивый к воздействию агрессивных веществ. Чтобы придать ему необходимые свойства, в металл добавляются различные легирующие компоненты в виде хрома, никеля, магния, титана и пр. Температура плавления нержавеющей стали по Цельсию составляет 1350-1500 градусов.
Ниже представлена таблица, в которой указана температура плавления жаропрочной нержавеющей стали наиболее популярных марок.
Жаропрочные стали и сплавы
Жаропрочная сталь используется при изготовлении разных деталей, которые контактируют с агрессивными средами, при этом подвергаются значительным нагрузкам, вибрациям и высокому термическому воздействию. К примеру, сюда относятся следующие изделия: турбины, печи, котлы, компрессоры и т.п. Далее представлены характеристики термостойких, жаропрочных сплавов, классификация, марки, особенности их применения.
Жаростойкая сталь (или окалиностойкая) – металлический сплав, используемый в ненагруженном или слабонагруженном состоянии и способный на протяжении длительного времени в условиях высоких температур (более 550 ºС) сопротивляться газовой коррозии. Жаропрочные металлы – изделия, которые под высоким термическим воздействием сохраняют свою структуру, не разрушаются, не поддаются пластической деформации. Важная характеристика таких металлов – условный предел ползучести и длительной прочности. Жаропрочные сплавы могут быть жаростойкими, однако не всегда такими бывают, поэтому в агрессивных средах могут быстро повредиться по причине окисления.
Свойства жаростойких и жаропрочных сплавов
Для повышения жаростойкости используются легирующие добавки, которые также улучшают прочность металлов. Благодаря легированию на поверхности сплавов образуется защитная пленка, снижающая скорость окисления изделий. Основные легирующие элементы: никель, хром, алюминий, кремний. В процессе нагрева образуются защитные оксидные пленки (Cr,Fe)2O3, (Al,Fe)2О. При содержании 5–8 % хрома жаростойкость стали увеличивается до 700–750 градусов по Цельсию, 17 % хрома – до 1000 градусов, при 25 % хрома – до 1100 градусов.
Жаропрочные марки металлов – сплавы на основе железа, никеля, титана, кобальта, упрочненные выделениями избыточных фаз (карбидов, карбонитридов и др.). Жаропрочностью обладают хромоникелевые и хромоникелевомарганцевые стали. Под воздействием высоких температур они не склонны к ползучести (медленная деформация при наличии постоянных нагрузок). Температура плавления жаропрочной стали составляет 1400-1500 °С.
Классификация жаропрочных и жаростойких сплавов
При температуре до 300 ºС используется обычная конструкционная (углеродистая) сталь – прочный и термостойкий металл. Для работы в условиях свыше 350 ºС требуется применение жаропрочных металлов. Основные виды сплавов повышенной термостойкости и термопрочности:
- Перлитные, мартенситные и аустенитные;
- кобальтовые и никелевые сплавы;
- тугоплавкие металлы.
К перлитным жаропрочным сталям относят котельные стали и сильхромы, содержащие малый процент углерода. Температура рекристаллизации материала повышается за счет легирования молибденом, хромом, ванадием. Сплавы характеризуются неплохой свариваемостью. Производство мартенситных сталей осуществляется с использованием перлитных и добавок хрома, закалки при 950–1100 ºС. Они содержат более 0,15 % углерода, 11-17 % хрома, небольшое количество никеля, вольфрама, молибдена, ванадия. Стали мартенситного класса устойчивы к воздействию коррозии в щелочных, кислотных растворах, повышенной влажности, в случае термообработки при 1050 градусах отличается высокой жаропрочностью.
Жаропрочные аустенитные стали могут иметь гомогенную или гетерогенную структуру. В сплаве с гомогенной структурой, не упрочняемых термообработкой, содержится минимум углерода, много легирующих элементов, что обеспечивает сопротивление ползучести. Такие материалы подходят для применения при температуре до 500 °С. В гетерогенных твердых растворах, упрочняемых термообработкой, образуются карбидные, интерметаллидные, карбонитридные фазы, что обеспечивает применение жаропрочных сплавов под напряжением при температуре до 700 °С.
При температуре до 900 °C эксплуатируют никелевые и кобальтовые сплавы: они применяются при производстве турбин реактивных двигателей, являются лучшими жаропрочными материалами. Кобальтовые сплавы по жаропрочности немного уступают никелевым, являются более редкостным. Отличаются высокой теплопроводностью, коррозионной устойчивостью при высоких температурах, стабильностью структуры в процессе длительной работы.
Содержание никеля в никелевом сплаве составляет свыше 55 %, углерода 0,06-0,12 %. В зависимости от структуры различают гомогенные (нихромы), гетерогенные (нимоники) сплавы никеля. Нихромы, изготавливаемые на основе никеля, в качестве легирующей добавки содержат хром. Им свойственна не только жаропрочность, но и высокая жаростойкость. Нимоники состоят из 20 % хрома, 2 % титана, 1 % алюминия. Марки сплавов: ХН77ТЮ, ХН55ВМТФКЮ, ХН70МВТЮБ.
При температурах до 1500 градусов и выше могут работать жаропрочные сплавы из тугоплавких металлов: вольфрама, ниобия, ванадия и др.
Стали по ГОСТ, классификация, свойства.
Классификация стали
Сталь – деформируемый (ковкий) сплав железа с углеродом (до 2%) и другими элементами. Это важнейший материал, который применяется в большинстве отраслей промышленности. Существует большое число марок сталей, различающихся по структуре, химическому составу, механическим и физическим свойствам. Посмотреть основные виды продукции металлопроката и ознакомиться с ценами можно здесь.
Основные характеристики стали:
- плотность
- модуль упругости и модуль сдвига
- коэффициент линейного расширения
- и другие
По химическому составу стали делятся на углеродистые и легированные. Углеродистая сталь наряду с железом и углеродом содержит марганец (0,1-1,0%), кремний (до 0,4%).
Сталь содержит также вредные примеси (фосфор, серу, газы — несвязанный азот и кислород). Фосфор при низких температурах придает ей хрупкость (хладноломкость), а при нагревании уменьшает пластичность. Сера приводит к образованию мелких трещин при высоких температурах (красноломкость).
Чтобы придать стали какие-либо специальные свойста (коррозионной устойчивости, электрические, механические, , магнитные, и т.д.), в нее вводят легирующие элементы. Обычно это металлы: алюминий, никель, хром, молибден, и др. Такие стали называют легированными.
Свойства стали можно изменять путем применения различных видов обработки: термической (закалка, отжиг), химико-термической (цементизация, азотирование), термо-механической (прокатка, ковка). При обработке для получения необходимой структуры используют свойство полиморфизма, присущее стали так же, как и их основе – железу. Полиморфизм – способность кристаллической решетки менять свое строение при нагреве и охлаждении. Взаимодействие углерода с двумя модификациями (видоизменениями) железа — α и γ – приводит к образованию твердых растворов. Избыточный углерод, не растворяющийся в α-железе, образует с ним химическое соединение — цементит Fe3C. При закалке стали образуется метастабильная фаза — мартенсит – пересыщенный твердый раствор углерода в α-железе. Сталь при этом теряет пластичность и приобретает высокую твердость. Сочетая закалку с последующим нагревом (отпуском), можно добиться оптимального сочетания твердости и пластичности.
По назначению стали делятся на конструкционные, инструментальные и стали с особыми свойствами.
Конструкционные стали применяют для изготовления строительных конструкций, деталей машин и механизмов, судовых и вагонных корпусов, паровых котлов. Инструментальные стали служат для изготовления резцов, штампов и других режущих, ударно-штамповых и измерительных инструментов. К сталям с особыми свойствами относятся электротехнические, нержавеющие, кислотостойкие и др.
По способу изготовления сталь бывает мартеновской и кислородно-конверторной (кипящей, спокойной и полуспокойной). Кипящую сталь сразу разливают из ковша в изложницы, она содержит значительное количество растворенных газов. Спокойная сталь — это сталь, выдержанная некоторое время в ковшах вместе с раскислителями (кремний, марганец, алюминий), которые соединяясь с растворенным кислородом, превращаются в оксиды и выплывают на поверхность массы стали. Такая сталь имеет лучший состав и более однородную структуру, но дороже кипящей на 10-15%. Полуспокойная сталь занимает промежуточное положение между спокойной и кипящей.
В современной металлургии сталь выплавляют в основном из чугуна и стального лома. Основные виды агрегатов для ее выплавки: мартеновская печь, кислородный конвертер, электропечи. Наиболее прогрессивным в наши дни считается кислородно-конвертерный способ производства стали. В то же время развиваются новые, перспективные способы ее получения: прямое восстановление стали из руды, электролиз, электрошлаковый переплав и т.д. При выплавке стали в сталеплавильную печь загружают чугун, добавляя к нему металлические отходы и железный лом, содержащий оксиды железа, которые служат источником кислорода. Выплавку ведут при возможно более высоких температурах, чтобы ускорить расплавление твердых исходных материалов. При этом железо, содержащееся в чугуне, частично окисляется:
2Fe + O2 = 2FeO + Q
Образующийся оксид железа (II) FeO, перемешиваясь с расплавом, окисляет, кремний, марганец, фосфор и углерод, входящие в состав чугуна:
Si +2FeO = SiO2 + 2 Fe + Q
Mn + FeO = MnO + Fe + Q
C + FeO = CO + Fe – Q
Чтобы довести до конца окислительные реакции в расплаве, добавляют так называемые раскислители – ферромарганец, ферросилиций, алюминий.
Марки стали
Марки стали углеродистой
Углеродистая сталь обыкновенного качества в зависимости от назначения подразделяется на три группы:
- группа А — поставляемая по механическим свойствам;
- группа Б — поставляемая по химическому составу;
- группа В — поставляемая по механическим свойствам и химическому составу.
В зависимости от нормируемых показателей стали группы А подразделяются на три категории: А1, А2, А3; стали группы Б на две категории: Б1 и Б2; стали группы В на шесть категорий: В1, В2, В3, В4, В5, В6. Для стали группы А установлены марки Ст0, Ст1, Ст2, Ст3, Ст4, Ст5, Ст6. Для стали группы Б марки БСт0, БСт1, БСт2, БСт3, БСт4, БСт5, БСт6. Сталь группы В изготовляется мартеновским и конвертерным способом. Для нее установлены марки ВСт2, ВСт3, ВСт4, ВСт5.
Буквы Ст обозначают сталь, цифры от 0 до 6 — условный номер марки стали в зависимости от химического состава и механических свойств. С повышением номера стали возрастают пределы прочности (σв) и текучести (σт) и уменьшается относительное удлинение (δ5).
Марку стали Ст0 присваивают стали, отбракованной по каким-либо признакам. Эту сталь используют в неответственных конструкциях.
В ответственных конструкциях применяют сталь Ст3сп.
Буквы Б и В указывают на группу стали, группа А в обозначении не указывается.
Если сталь относится к кипящей, ставится индекс «кп», если к полустойкой — «пс», к спокойной — «сп».
Качественные углеродистые конструкционные стали применяют для изготовления ответственных сварных конструкций. Качественные стали по ГОСТ 1050-74 маркируются двузначными цифрами, обзначающими среднее содержание углерода в сотых долях процента. Например, марки 10, 15, 20 и т.д. означают, что сталь содержит в среднем 0,10%, 0,15%, 0,2% углерода.
Сталь по ГОСТ 1050-74 изготовляют двух групп: группа I — с нормальным содержанием марганца (0,25-0,8%), группа II — с повышенным содержанием марганца (0,7-1,2%). При повышенном содержании марганца в обозначение дополнительно вводится буква Г, указывающая, что сталь имеет повышенное содержание марганца.
Марки стали легированной
Легированные стали кроме обычных примесей содержат элементы, специально вводимые в определенных количествах для обеспечения требуемых свойств. Эти элементы называются лигирующими. Лигированные стали подразделяются в зависимости от содержания лигирующих элементов на низколегированные (2,5% легирующих элементов), среднелегированные (от 2,5 до 10% и высоколегированные (свыше 10%).
Лигирующие добавки повышают прочность, коррозийную стойкость стали, снижают опасность хрупкого разрушения. В качестве легирующих добавок применяют хром, никель, медь, азот (в химически связанном состоянии), ванадий и др.
Легированные стали маркируются цифрами и буквами, указывающими примерный состав стали. Буква показывает, какой легирующий элемент входит в состав стали (Г — марганец, С — кремний, Х -хром, Н — никель, Д — медь, А — азот, Ф — ванадий), а стоящие за ней цифры — среднее содержание элемента в процентах. Если элемента содержится менее 1%, то цифры за буквой не ставятся. Первые две цифры указывают среднее содержание углерода в сотых долях процента.
Нержавеющая сталь. Свойства. Химический состав
Нержавеющая сталь — легированная сталь, устойчивая к коррозии на воздухе, в воде, а также в некоторых агрессивных средах. Наиболее распространены хромоникелевая (18% Cr b 9%Ni) и хромистая (13-27% Cr) нержавеющая сталь, часто с добавлением Mn, Ti и других элементов.
Добавка хрома повышает стойкость стали к окислению и коррозии. Такая сталь сохраняет прочность при высоких температурах. Хром входит также в состав износостойких сталей, из которых делают инструменты, шарикоподшипники, пружины.
Примерный химический состав нержавеющей стали ( в %)